Традиционно хроническая обструктивная болезнь легких (ХОБЛ) считалась болезнью легких, сопровождающейся хронической бронхиальной обструкцией и прогрессирующими структурными изменениями в дыхательных путях (бронхит) и в паренхиме легких (эмфизема). Была установлена связь структурных изменений с воспалительной реакцией в дыхательных путях, альвеолах и легочных сосудах. Однако воспалительная реакция обнаруживается и в системном кровотоке, что проявляется повышением количества лейкоцитов в крови, уровня острофазовых белков (С-реактивного белка и фибриногена), интерлейкина-6 (ИЛ-6), фактора некроза опухолей (ФНО-α) в сыворотке крови. Многочисленными исследованиями подтверждается, что системное воспаление вносит значительный вклад в патогенез экстрапульмональных проявлений болезни, так называемых системных эффектов. К наиболее значимым системным эффектам хронической обструктивной болезни легких относят потерю массы тела, мышечную дисфункцию, повышенный риск сердечно-сосудистых заболеваний, остеопороз, анемию, депрессию.
Клиническое и прогностическое значение системных эффектов хронической обструктивной болезни легких представлено в Глобальной стратегии диагностики, лечения и профилактики хронической обструктивной болезни легких, пересмотренной в 2007 г. рабочей группой GOLD (Global Initiative for Chronic Obstructive Lung Disease). Таким образом, дефиниция ХОБЛ в настоящее время выглядит следующим образом: хроническая обструктивная болезнь легких — заболевание, которое характеризуется хроническим ограничением скорости воздушного потока, разнообразными патологическими изменениями в легких, существенными внелегочными проявлениями и серьезными сопутствующими заболеваниями, которые могут дополнительно отягощать течение ХОБЛ. Выраженность системных проявлений увеличивается с прогрессированием обструкции, поэтому указанные проявления часто недооцениваются и становятся очевидными на поздних стадиях болезни. Системные проявления снижают качество жизни, способствуют ранней инвалидизации и вносят значительный вклад в смертность больных с ХОБЛ. Одним из наиболее серьезных и социально значимых системных проявлений хронической обструктивной болезни легких является остеопороз.
В настоящее время остеопороз рассматривается как заболевание скелета, при котором снижена прочность кости и повышен риск переломов. В этиопатогенетической классификации остеопороза, принятой на заседании президиума Российской ассоциации по остеопорозу в январе 1997 г., хроническая обструктивная болезнь легких указывается как одна из причин вторичного остеопороза.
Ведущую роль в патогенезе остеопороза при ХОБЛ играет системное воспаление, которое ассоциировано с продукцией хемоаттрактантов и маркеров воспаления. Результаты научных исследований свидетельствуют о повышении уровня С-реактивного белка, фибриногена, ИЛ-6, ФНО-α, растворимых рецепторов типов 1 и 2 ФНО-α. Предполагается, что провоспалительные цитокины ФНО-α и ИЛ-6 могут стимулировать остеокласты и усиливать резорбцию костной ткани, способствуя тем самым развитию остеопороза. Системное воспаление при ХОБЛ приводит также к усилению катаболизма белков. У пациентов с ХОБЛ происходит снижение количества нежировой ткани и повышение каталитической активности ферментов, приводящее к мышечной дисфункции и потере костной массы. Возможные механизмы развития остеопороза у больных ХОБЛ представлены на рис. 1.
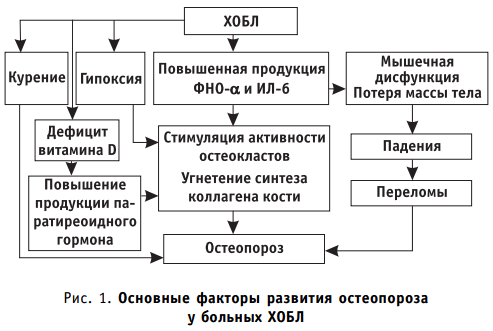
Остеопороз у больных ХОБЛ часто не диагностируется, так как развивается постепенно и в течение долгого времени остается бессимптомным, а внимание врачей обращено на респираторную симптоматику и функциональные показатели. Тем не менее, остеопороз с возможными переломами является важной проблемой для пациентов с ХОБЛ. Переломы сопровождаются болевым синдромом, ограничением физической активности, снижением качества жизни, способствуют ухудшению респираторной функции, являются причиной временной нетрудоспособности, инвалидизации и смертности. Наиболее характерными для остеопороза у больных ХОБЛ являются компрессионные переломы позвоночника (чаще грудного отдела), которые могут приводить к увеличению грудного кифоза и вторично влиять на респираторную функцию. Несмотря на то, что переломы чаще случаются у пациентов с выраженной степенью хронической обструктивной болезни легких, выявление остеопений на начальных стадиях позволяет принять превентивные меры и снизить риск переломов.
Диагностика
«Золотым стандартом» диагностики остеопороза считается двухэнергетическая рентгеновская абсорбциометрия — dual energy X-ray absorptiometry (DXA), так как при небольшой дозе облучения можно исследовать важные в плане остеопороза отделы скелета. Метод основан на измерении степени ослабления костной тканью пучка рентгеновского излучения при линейном сканировании позвонков и шейки бедренной кости. При проведении денситометрии методом DXA оценивается количество минерализованной костной ткани в сканируемой площади (в г/см2); кроме того, полученные результаты сравниваются с референсной базой данных и представляются в виде Т-критерия (количество стандартных отклонений выше или ниже среднего показателя пиковой костной массы молодых женщин) и Z-критерия (количество стандартных отклонений от возрастной нормы). В 1994 г. группой экспертов ВОЗ были сформулированы диагностические критерии остеопороза (табл. 1), которые основаны на количественной оценке минеральной плотности кости различных областей скелета по Т-критерию.
Таблица 1.
Критерии остеопороза (ВОЗ, Женева, 1994)
| Категория | Значения Т-критерия |
| Норма | Более-1 стандартного отклонения |
| Остеопения | От -1 до -2,5 стандартных отклонений |
| Остеопороз | -2,5 стандартных отклонения и ниже |
| Тяжелый остеопороз | -2,5 стандартных отклонения и ниже с наличием в анамнезе 1 и более переломов |
Ультразвуковая денситометрия, в частности, костная ультрасонометрия (КУС) позволяет исследовать только кости периферического скелета. Кроме того, ультразвуковые денситометры не стандартизированы, не определены для них значения Т-критерия, соответствующие остеопении и остеопорозу, поэтому их нельзя рассматривать в качестве инструмента для количественной диагностики снижения минеральной плотности кости (МПК), они не являются альтернативой DXA при скрининге, результаты костной ультрасонометрии не могут служить основанием для назначения лечения остеопороза и контроля за его эффективностью.
При количественной компьютерной томографии производится трехпространственное измерение минеральной плотности кости c определением количества минерализованной костной ткани на объем кости в г/см3, однако в клинической практике метод не нашел широкого распространения.
Рентгенологическое исследование костей скелета в настоящее время рекомендуется использовать только для диагностики переломов костей любой локализации и для дифференциальной диагностики заболеваний скелета, так как рентгенологические признаки остеопороза проявляются только при потере 30-40% костной массы.
При диагностике остеопороза важна также оценка метаболизма костной ткани. Для этого используются показатели фосфорно-кальциевого обмена и биохимические маркеры костного метаболизма. К обязательным методам исследования относят определение в крови уровня общего или ионизированного кальция, фосфора, магния, а также исследование суточной экскреции кальция и фосфора или их исследование в моче натощак по отношению к экскреции креатинина; паратиреоидный гормон и активные метаболиты витамина D определяются по строгим показаниям. Биохимические маркеры костного метаболизма исследуют для оценки скорости процессов костного ремоделирования и выявления разобщенности костной резорбции и костеобразования.
К маркерам костеобразования относят активность общей щелочной фосфатазы в крови и ее костного изофермента, остеокальцин (синтезируемый остеобластами), карбокси- и аминоконцевые пропептиды проколлагена 1 типа.
К маркерам резорбции костной ткани относят экскрецию оксипролина с мочой, активность кислой тартратрезистентной фосфатазы и определение продуктов распада коллагена: пиридинолина, дезоксипиридинолина, N- и C-концевых телопептидов. В настоящее время в Республике Беларусь определяются такие маркеры костного метаболизма, как щелочная фосфатаза, остеокальцин и С-телопептид (β-CTX).
Доказано, что у больных ХОБЛ, получающих ингаляционные глюкокортикостероиды в течение года, выявлялся достоверно более низкий уровень остеокальцина (р < 0,0001), кальция (р < 0,004) и кортизола (р < 0,026) в сыворотке крови, чем в группе контроля. Изучалось также влияние беклометазона и будесонида на костный метаболизм и минеральную плотность кости. При этом выявлено, что оба препарата снижали уровни маркеров костеобразования остеокальцина и С-концевого пропептида проколлагена I типа, но на повышение уровня маркера костной резорбции С-концевого телопептида коллагена I типа и снижение минеральной плотности кости больше влиял беклометазон. Минеральная плотность кости нелеченных больных ХОБЛ отрицательно коррелировала с уровнем С-концевого телопептида коллагена типа I, маркера костной резорбции (r = −0,444; р < 0,001), но не коррелировала с уровнем остеокальцина, маркера костеобразования, что свидетельствует об усилении процессов резорбции у этой группы пациентов.
Одним из наиболее информативных методов диагностики и дифференциальной диагностики остеопороза является биопсия костной ткани из гребня крыла подвздошной кости с последующим гистоморфометрическим исследованием, что позволяет различить остеопороз и другие виды патологии костной ткани, а также охарактеризовать тип обмена в костной ткани.
Лечение и профилактика
В настоящее время не существует руководств по профилактике и лечению остеопороза у больных ХОБЛ. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких не содержит каких-либо рекомендаций по лечению остеопороза у этой группы пациентов. Согласно имеющимся рекомендациям Российской ассоциации по остеопорозу, основными направлениями профилактики остеопороза являются обеспечение полноценного питания с достаточным количеством кальция, фосфора, витаминов и минералов, поддержание физической активности, отказ от вредных привычек (курение, алкоголь), предупреждение падений, фармакопрофилактика, создание образовательных программ.
Применяющиеся для лечения и профилактики остеопороза лекарственные средства по механизму действия подразделяют на препараты, замедляющие костную резорбцию (эстрогены, селективные модуляторы эстрогеновых рецепторов, бисфосфонаты, кальцитонины, кальций), стимулирующие костеобразование (фториды, паратиреоидный гормон, гормон роста, анаболические стероиды, андрогены) и препараты, обладающие многоплановым действием (витамин D и его активные метаболиты, оссеин-гидроксиаппатитный комплекс, соли стронция).
Обязательным компонентом любой схемы профилактики и лечения остеопороза является адекватное употребление кальция и витамина D, содержащихся в пищевых продуктах и лекарственных препаратах.
Известно, что назначение заместительной гормональной терапии женщинам в постменопаузе снижает риск переломов. Выявлено также, что у женщин, принимающих глюкокортикостероиды (ГКС), лечение эстрогенами или прогестероном уменьшает скорость потери минеральной плотности кости. Дефицит тестостерона у мужчин с ХОБЛ, усугубляющийся на фоне лечения системными глюкокортикостероидами, является одним из факторов развития остеопороза у данной категории пациентов. С учетом снижения мышечной массы у больных ХОБЛ и катаболического эффекта глюкокортикостероидов назначение тестостерона может иметь еще и дополнительные показания для увеличения мышечной массы и снижения жировой ткани.
Кальцитонин тормозит резорбцию кости за счет угнетения активности остеокластов, а также обладает анальгетическим эффектом. При применении кальцитонина в большей степени наблюдается улучшение качества кости, чем увеличение показателей минеральной плотности кости, что приводит, тем не менее, к снижению риска вертебральных переломов.
Бисфосфонаты подавляют резорбцию костной ткани, обладают доказанной эффективностью в повышении минеральной плотности кости и снижении риска переломов, могут использоваться для профилактики и лечения различных форм остеопороза. Получены данные, что применение ризедроната предотвращает потерю минеральной плотности кости при длительном применении глюкокортикостероидов. Так, у принимающих плацебо снижение минеральной плотности кости составило 2,8%, а у принимающих 5 мг ризедроната наблюдался прирост минеральной плотности кости (0,6%). Небольшое количество исследований посвящено изучению эффективности лечения остеопороза бисфосфонатами у больных пульмонологического профиля. В исследовании B. J. Smith et al. проводилось изучение влияния алендроната на минеральную плотности кости у больных легочными заболеваниями. У принимавших алендронат/кальций (10 мг / 600 мг в день) в течение 12 месяцев выявлено повышение минеральной плотности кости в поясничном отделе позвоночника по сравнению с принимавшими плацебо/кальций; изменений минеральной плотности кости бедра не наблюдалось.
Стронция ранелат способствует формированию костной ткани и, одновременно, предотвращает резорбцию кости, оказывая двойное действие на костное ремоделирование. Препарат существенно повышает минеральную плотности кости, а также обладает доказанной эффективностью в отношении снижения риска как вертебральных, так и невертебральных переломов.
Заключение
Представленный обзор литературы демонстрирует повышенный риск возникновения остеопороза у пациентов с ХОБЛ. Поэтому при наличии дополнительных факторов риска (низкая масса тела, выраженная дыхательная недостаточность, низкая физическая активность, переломы в анамнезе, прием системных и ингаляционных глюкокортикостероидов) у больных ХОБЛ необходим мониторинг минеральной плотности кости для раннего выявления потери костной массы. Своевременная профилактика и лечение остеопороза позволяют предотвратить переломы, которые снижают качество жизни больных, увеличивают заболеваемость и смертность.
Харевич О. Н., Лаптева И. М., Никитина Л. И., Лаптева Е. А.
Республиканский научно-практический центр пульмонологии и фтизиатрии, Республиканский клинический медицинский центр Управления делами Президента Республики Беларусь.
Журнал «Медицинская панорама» № 9, октябрь 2009.